质子交换膜燃料电池(PEFCs)作为一种具有潜力的能源转换装置,尤其在汽车应用中展现出广阔前景。然而,PEFCs的有限服务寿命被认为是燃料电池电动汽车(FCEVs)广泛商业化的主要障碍。近期的研究表明,PEFCs的性能在很大程度上依赖于其各个组件的状态。
PEFCs由具有高离子导电性的电解质膜、两侧配备铂/碳(Pt/C)催化剂的多孔电极以及气体扩散层(GDL)组成。通常,已有研究报告指出多种降解现象,如电解质膜的分解及电极活性在燃料电池反应中的劣化。实际上,导致降解的反应受到操作条件的影响,并且其发生过程相当复杂;因此,PEFCs的降解机制至今尚未完全明晰。
特别是,由于纳米颗粒的聚集与溶解,以及铂从碳载体上的脱离,铂催化剂的电化学表面积(ECSA)在燃料电池运行过程中会减少,从而导致阴极氧还原反应(ORR)速率下降,进而引发整体性能的衰退。
在Pt/C催化剂失活的原因中,表面氧化层的形成、磺酸根离子(SO3-)的吸附,以及一氧化碳(−CO)、二氧化硫(−SO2)等杂质的存在,都会使氧气难以与表面铂上的质子和电子发生反应,从而导致阴极动力学变得迟缓。由于这些性能损失通常被视为不可逆降解,因此,针对已降解Pt/C催化剂的再激活研究仍然较为匮乏。
汽车应用要求PEFCs能够快速适应变化的操作条件;加速和减速引起的负载变化会导致PEFCs电位波动,频繁的启停操作则会导致电位剧烈变化。近期的研究表明,在阴极侧,Pt/C催化剂在经历反复的电位循环时,降解程度比在恒定电位保持条件下更为严重。
01 碳载体的可逆/不可逆降解机制
碳载体的劣化被认为是催化剂降解的主要原因之一。图1展示了在阴极电位下碳载体的氧化机制。通过缺陷位点(defect sites)的水解反应(hydrolysis reaction)生成醇类物质,被认为是碳载体电化学氧化的初始反应。在碳气化为二氧化碳(CO2)之前,羧基(carboxylic)和内酯基团(lactones groups)是通过羰基的氧化形成的。在碳氧化过程中,除了醌醇(C-OH)与醌(C=O)之间的氧化还原反应外,一旦链结构断裂,实际上无法通过羧基的形成重建碳的结构。

02 铂的可逆/不可逆降解机制
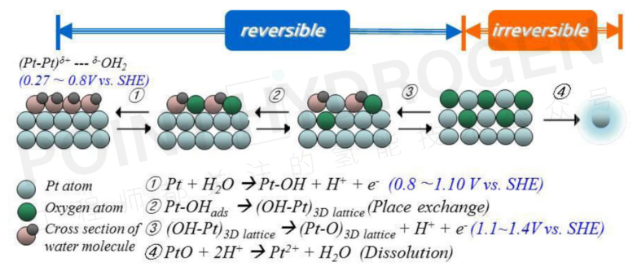
与碳氧化机制相反,大多数铂表面氧化反应是可逆进行的,如图2所示(反应1至3),直到铂通过铂氧化物(PtO)的化学溶解或金属铂的电化学氧化转变为Ptn+(n=2,4)为止。因此,作为氧化过程中间体存在的铂氧化物(Pt-Ox,-OH,-O)可以在典型操作条件下被电化学还原。
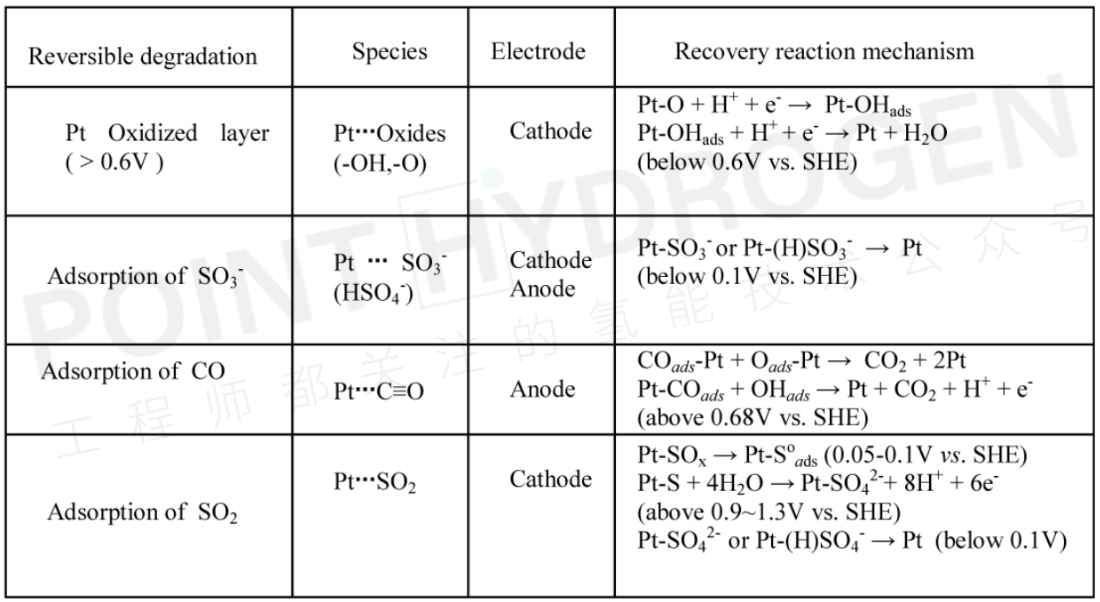
除了Pt-Ox外,典型的杂质,如一氧化碳(−CO)、二氧化硫(−SO2),也是在实际汽车应用中导致Pt/C催化剂失活的来源。表1总结了根据不同吸附物种的恢复反应机制。